- TENSION ARTÉRIELLE
- TENSION ARTÉRIELLEC’est par un abus de langage, consacré par l’usage, que les médecins et le public parlent de tension artérielle (et d’«hypertension»), alors que, sous ce vocable, ils désignent la pression qui règne à l’intérieur du compartiment artériel. Celle-ci est facile à mesurer dans ce compartiment à haute pression, à faible compliance, qui contient seulement 15 p. 100 du volume sanguin total. Chaque systole cardiaque emmagasine sous une certaine pression un certain volume de sang oxygéné distribué par le jeu des vannes artériolaires là où il est nécessaire.Quand un ingénieur parle de la tension qui règne dans la paroi d’un tuyau, il considère la force qui tend à étirer cette paroi. Avec L. E. Peterson, on peut écrire que la tension T est unie à la pression P qui règne dans le vaisseau, à son rayon r et à son épaisseur 嗀 par la relation:
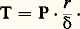 La tension est donc une force par unité de surface. Quand un médecin parle de tension artérielle, il envisage, en fait, la pression artérielle (P), dont, pour une artère de rayon et d’épaisseur donnés, dépend la tension du vaisseau.Les conceptions cybernétiques permettent une formalisation heuristique. Un système de régulation à court terme utilise les afférences venues de récepteurs à l’étirement (placés dans les sinus carotidiens) pour moduler, à chaque instant, l’activité cardiaque, le degré d’ouverture des vannes artériolaires, la compliance du réservoir veineux.Le remplissage du système circulatoire est contrôlé essentiellement, pour l’eau, par le jeu de l’hormone antidiurétique (réglé à partir d’osmorécepteurs et de volorécepteurs) et, pour le sodium, par l’intervention de l’aldostérone, hormone corticosurrénale dont la sécrétion est, en grande partie, asservie au taux d’angiotensine fabriquée par une enzyme d’origine rénale: la rénine.Les connaissances physiologiques acquises permettent désormais de remédier directement aux causes de l’hypertension artérielle et, dans la grande majorité des cas, d’opposer des médications efficaces à cette anomalie physiopathologique aux conséquences redoutables.1. Physiologie de la pression artérielleHistoriqueIl a fallu plus de cent ans, après que Harvey eut découvert la circulation du sang (1628), pour que S. Hales mesure pour la première fois la pression artérielle (1730), grâce à un tube de verre relié à une canule placée dans l’artère crurale d’une jument; un autre siècle s’écoule avant que J. L. M. Poiseuille applique à l’étude de la pression artérielle sanguine le manomètre à mercure (1828); la notion de pression était déjà bien précisée (une force rapportée à une surface) et, aujourd’hui encore, les physiologistes ont conservé l’habitude d’évaluer en millimètres de mercure plutôt qu’en unités C.G.S.C. F. Ludwig, vers 1847, met au point le «kymographion», qui permet de tracer le graphe de la pression artérielle (en millimètres de mercure) en fonction du temps. E. J. Marey et A. Chauveau, vers 1860, inventent les dispositifs qui rendent possible l’étude des variations de pressions à l’intérieur de l’appareil circulatoire. L’époque contemporaine a vu enfin la réalisation de capteurs convertissant l’énergie mécanique en signaux électriques auxquels on peut faire subir toutes les transformations qu’implique maintenant le traitement de l’information (P. Laurens).Chez l’homme, les méthodes de mesure non sanglante de la pression artérielle (par l’intermédiaire de la contre-pression instituée sur les troncs artériels des membres grâce à un brassard de caoutchouc gonflable) font partie de la routine clinique. Les méthodes palpatoires de S. Riva Rocci (1896), oscillatoires de V. Pachon (1909) sont moins utilisées que la méthode auscultatoire de P. Korotkow (1905) qui s’appuie sur l’étude des caractéristiques des bruits artériels synchrones avec la pulsation artérielle. Ces diverses méthodes mesurent en fait l’aptitude de la paroi vasculaire à équilibrer (par son élasticité) la pression sanguine: elles permettent ainsi d’évaluer la pression artérielle et de mettre en évidence ses variations normales et pathologiques.Données physiologiquesLes variations de la pression artérielleOn résumera ici les faits exposés déjà dans l’article appareil CIRCULATOIRE. Si l’on enregistre simultanément une courbe de pression intraventriculaire gauche et l’électrocardiogramme, on constate la succession des phénomènes suivants:– l’onde rapide Q.R.S.T. de l’électrocardiogramme (50 ms) précède tous les phénomènes mécaniques;– pendant la contraction isométrique ventriculaire (50 ms), la pression intraventriculaire croît sans que la pression aortique monte;– pendant la période d’éjection ventriculaire (220 ms), les courbes ventriculaires et aortiques coïncident: la pression aortique maximale peut être identifiée à la pression systolique ventriculaire;– la pression aortique décrit un ressaut (l’incisure) à la fin de l’éjection ventriculaire: la fermeture des sigmoïdes aortiques sépare les régimes de pression aortique et ventriculaire; là commence la diastole cardiaque; la pression aortique décroît progressivement jusqu’à un minimum qui coïncide avec la fin de la diastole cardiaque et pour cette raison est appelée pression diastolique.À ces oscillations de premier ordre se superposent des oscillations de deuxième ordre en rapport avec les mouvements respiratoires, et les oscillations dites de Traube-Hering qui surélèvent l’ensemble du tracé à une fréquence beaucoup plus lente (W. D. Halliburton).Modifications de la pression sanguine dans l’appareil circulatoireChez l’homme, les performances sont obtenues grâce à la convexion forcée que réalise la pompe cardiaque à l’intérieur de la tuyauterie vasculaire en circuit fermé.En suivant le circuit circulatoire, on peut distinguer un certain nombre de segments à propriétés très contrastées (cf. appareil CIRCULATOIRE, fig. 9).Le compartiment à haute pression commence avec le ventricule gauche (lors de la systole) et s’étend jusqu’aux artérioles. Ce compartiment contient seulement une faible proportion du volume sanguin (environ 15 p. 100); son volume ne dépend pas du volume sanguin total mais de celui qui est éjecté à la systole par le ventricule gauche et de l’élasticité des vaisseaux ; il présente une faible compliance (la compliance est définie, grâce au nombre de litres mobilisés par une variation de pression unité); il est drainé par des systèmes artériolaires, disposés en parallèle, dont la résistance est réglée par l’action de cellules musculaires lisses.Il semble que la stabilisation de la pression artérielle ait pour but téléonomique la perfusion correcte des organes nobles «servis et non asservis», le cœur et le cerveau, aux dépens de la fermeture éventuelle d’autres shunts artério-veineux.Viennent ensuite le compartiment de distribution capillaire et cellulaire et le compartiment à basse pression qui contient environ 80 p. 100 du volume sanguin: 55 p. 100 dans les veines et les veinules; le reste, soit 25 p. 100 de la masse sanguine, dans le cœur droit, les poumons et l’oreillette gauche.Interprétation cybernétiqueDepuis que les travaux de Wiener sur la cybernétique ont formalisé l’idée de rétro-action, les physiologistes se sont efforcés de formaliser la structure logique du système de régulation de la pression artérielle.Supposons, dans un premier temps, que le remplissage du système schématisé dans la figure 1 soit convenable et stable: la pression artérielle est la grandeur réglée à l’intérieur du système (en trait gras); elle dépend de l’interaction entre la pompe cardiaque, qui réalise la charge du système, et le calibre des artérioles, qui décide du débit de drainage. Soit un capteur sensible à l’étirement situé dans l’intimité de la paroi du système réglé qui renseigne à chaque instant un système comparateur (comportant une grandeur de consigne GC): ce sera la boucle de rétroaction négative du système cybernétique. L’écart entre la grandeur de consigne et la grandeur mesurée par le capteur constitue l’information qui permet au contrôleur d’asservir pompe cardiaque et résistances artériolaires.Aux «entrées utiles», réseau de communication qui unit le système de contrôle aux deux effecteurs cardiaque et vasculaire constituant le système réglant, s’opposent des «entrées parasites» qui peuvent, à chaque instant, déséquilibrer l’ensemble. Les entrées sont liées à l’activité cellulaire, glandulaire ou musculaire, aboutissant à la synthèse d’un certain nombre de substances vaso-activesdites «autacoïdes» par Sharpey Schafer (sérotonine, histamine, prostaglandines). C’est probablement par l’intermédiaire de telles substances (et aussi de la pression artérielle de gaz carbonique) que les circulations locales «négocient» les données imposées par la régulation générale, qui doit alors, par le jeu des rétroactions, déterminer un nouvel équilibre.Régulation «immédiate» de la pression artérielleAnalyse des afférences barosensibles: les nerfs dépresseursEn 1867, E. de Cyon et C. F. Ludwig découvrent un «nerf dépresseur» (fig. 2); prenant son origine au niveau de la crosse aortique et dont l’excitation détermine bradycardie et hypotension. Mais ce sont les travaux de H. E. Hering (1924) qui apportent les repères essentiels. La compression du sinus carotidien détermine une chute de la pression sanguine avec ralentissement du rythme cardiaque; ces phénomènes ne se produisent pour aucun autre segment des carotides. Les mêmes résultats sont obtenus par étirement des sinus de dedans en dehors par un ballonnet ou par augmentation de la pression sanguine à l’intérieur du sinus. Les terminaisons des nerfs de Hering ne sont pas sensibles directement à la pression; si l’on entoure la paroi du sinus d’une feuille de plomb, les modifications de pression à l’intérieur ne déterminent plus de réponse; les récepteurs sont des récepteurs à la distorsion de la paroi. Tous ces effets sont abolis par la section d’un rameau nerveux (appelé ordinairement nerf de Hering) qui joint le sinus carotidien au glosso-pharyngien. La stimulation du bout central de ce nerf entraîne les mêmes effets que la déformation de la paroi du sinus.Si l’on coupe les nerfs de Cyon et les nerfs de Hering, la pression artérielle s’installe (comme Hering l’a montré pour le chien) à un niveau très élevé. Il faut admettre qu’à chaque instant ces nerfs exercent une action dépressive sur le système cardio-vasculaire, ils sont bien les «rênes de la pression sanguine» (Blutdruckzügler ).Étude des «ripostes»Si l’on déclenche la réaction du système «à boucle ouverte» en excitant le nerf du sinus ou en distendant le sinus, selon la technique de J. Heymans, cette réaction s’exerce au niveau des deux systèmes asservis: la pompe cardiaque, les shunts artériolaires (fig. 2).La pompe cardiaque est douée d’une parfaite autonomie: un cœur isolé dans des conditions convenables conserve son activité rythmique et mécanique et s’adapte au débit qui lui est apporté (cf. infra ). Mais, dans l’organisme entier, il est asservi par l’intermédiaire des neuromédiateurs que lui délivrent les systèmes parasympathiques (nerfs pneumogastriques ou vagues) et orthosympathiques (avec le relais médullo-surrénal). La vagotomie, ou l’administration d’atropine, empêche le ralentissement cardiaque déclenché par l’excitation du nerf du sinus carotidien; celle-ci inhibe, d’autre part, l’accélération du rythme cardiaque par les nerfs cardiaques orthosympathiques. Au contraire, la section des nerfs du sinus les empêche de réfréner l’activité orthosympathique qui, par l’intermédiaire des récepteurs cardiaques de type 廓 (c’est-à-dire bloqués électivement par des drogues du type propanolol), aboutissent à l’accélération du cœur et à l’augmentation de la force de ses battements.Les artérioles , de leur côté, sont douées d’autorégulation probablement myogène (B. Folkow): toute augmentation brusque de la perfusion d’une artère isolée in vitro détermine une réponse constrictrive, peut-être par le truchement de certaines cellules musculaires de la paroi du vaisseau; douées d’autonomie, elles ont été appelées «unitaires» (E. Bozler). Mais, en dehors de ces phénomènes d’autorégulation, la plupart des cellules musculaires du vaisseau (dites multi-unitaires) sont asservies par le truchement de fibres végétatives. Le rôle essentiel en matière de réponse vaso-motrice, à la suite de la distension des sinus, est joué par la diminution du tonus vaso-constricteur que maintient la noradrénaline libérée par les terminaisons orthosympathiques au contact des alpha-récepteurs des fibres musculaires lisses des artérioles (rappelons que ces récepteurs sont bloqués par l’ergotoxine et la phentolamine). Les fibres vasodilatatrices (orthosympathiques cholinergiques) ne participent pas à cette régulation (B. Folkow et B. Uvnäs).Reste à situer l’importance du réservoir veineux : une diminution du calibre veineux, par exemple, va augmenter le retour veineux au niveau du cœur et déterminer l’allongement des fibres cardiaques et la réponse adaptée, propre à ces fibres. Ce mécanisme d’ajustement, fonction de la longueur diastolique des fibres, est un ajustement a posteriori, curatif, qui peut s’ajouter au contrôle homéométrique préventif réalisé (cf. supra , Interprétation cybernétique ) par le truchement des catécholamines sécrétées par le système végétatif.De toute façon, le contrôle neurovégétatif découle de l’activité de centres nerveux spécialisés. On peut mettre en évidence leur localisation et leur rôle par ablation localisée ou par stimulation (avec le risque d’obtenir des réponses par des voies qui ne sont pas physiologiques). On met ainsi en évidence des centres bulbaires (noyaux des IXe et Xe paires crâniennes en particulier), suprabulbaires et médullaires. Au niveau de ces nerfs reliés à ces centres, les ganglions latérovertébraux sont le siège des relais synaptiques. La médullo-surrénale représente, pour le nerf grand-splanchnique, l’équivalent de cellules ganglionnaires qui sécrètent les catécholamines (adrénaline surtout) dans le système circulatoire par lequel elles gagnent la pompe cardiaque et les drains artériolaires.On peut imaginer a priori que l’ajustement réflexe varie soit en fonction d’un «resetting» de la valeur de consigne décidé au niveau des centres par le contrôleur (fig. 1), soit en fonction de modifications des propriétés mécaniques de la paroi des sinus.Régulation du remplissageEn fonction de la diurèse nécessaire à l’activité rénale, des pertes par perspiration cutanée et respiratoire, la «masse sanguine» varie. Une modulation de la fonction rénale et du ravitaillement oral va la régler suivant des mécanismes «à long terme» (à grande constante de temps). Le «remplissage» (fig. 3) concerne essentiellement le compartiment compliant, c’est-à-dire l’ensemble de la tuyauterie vasculaire, à l’exception du cœur gauche en systole et du système artériel dont on a étudié la régulation. L’osmolarité et la volémie sont réglées en même temps, mais, s’il le faut, l’osmolarité est sacrifiée au maintien de la volémie.Hormone antidiurétique et eauDepuis E. B. Verney, on sait que l’on bloque la diurèse déterminée par un apport d’eau par voie buccale en injectant une faible quantité de solution salée hypertonique dans la carotide (sans action par une autre voie). On a reconstruit (fig. 3) le circuit qui, par le jeu d’osmorécepteurs (a ), met en route la sécrétion, par des neurones supraoptiques, d’hormone antidiurétique (ADH), libérée au niveau de la posthypophyse dans le torrent circulatoire pour agir au niveau du tube distal du néphron [cf. REIN] en favorisant la réabsorption d’eau. Ainsi est rétablie par feed-back négatif l’osmolarité normale. Ce contrôle de l’osmolarité par le jeu de l’ADH est coiffé par des volorécepteurs, certains situés dans la veine cave (réflexe de Bainbridge, b ), d’autres (discutés) dans l’oreillette et dans le ventricule (réflexe de Bezold Jarisch, b -b ). Mais les plus importants sont ceux situés dans l’oreillette gauche (c ) et décrits par O. J. Gauer et J. P. Henry. Ces capteurs de l’oreillette gauche sont excités par la distension suivant un mécanisme analogue à celui que nous avons vu au niveau du sinus carotidien. Les informations cheminent cette fois-ci par la voie afférente du pneumogastrique: au niveau des centres supraoptiques l’embargo est mis sur l’exportation d’ADH. Se déclenche ainsi une diurèse qui empêche que la pression ne favorise, dans le secteur intrathoracique, une exsudation œdémateuse au niveau des alvéoles pulmonaires.Systèmes aldostérone et sodium. Systèmes rénauxOn sait, depuis Tigerstedt et Bergman, (1898) que le rein règle la pression artérielle par l’intermédiaire d’une substance humorale, la rénine. Les travaux des écoles de I. H. Page (1939) et de E. Braun-Ménendez (1940) ont montré que la rénine est une enzyme qui agit sur une 見-2-globuline plasmatique pour fabriquer un décapeptide, l’angiotensine I , que la traversée pulmonaire transforme en un octapeptide de structure chimique connue: l’angiotensine II. Il y a tout lieu de penser que ce sont certaines cellules myocytaires à granules cytoplasmiques de l’artère afférente du glomérule qui sécrètent la rénine. Tout se passe comme si de la diminution de la pression artérielle provoquant l’excitation sécrétoire des cellules à granules résultait une concentration plus élevée de rénine, c’est-à-dire d’angiotensine. Celle-ci est non seulement une substance artériolo-constrictrice, mais, de plus, elle déclenche, comme J. Genest, puis J. H. Laragh l’ont démontré, la sécrétion d’aldostérone par le cortex surrénalien. Sous l’action de l’aldostérone sécrétée, le tube contourné distal réabsorbe davantage de sodium conduisant à l’inflation du compartiment extracellulaire, vasculaire en particulier, c’est-à-dire au rétablissement d’une «pression normale».D’autres facteurs agissent au niveau du rein et contribuent à cette régulation: l’équilibre ou «balance» glomérulo-tubulaire; l’intervention constrictrice de prostaglandines sur l’artère efférente du glomérule et l’action natriurétique d’un éventuel «troisième facteur», s’ajoutant à l’aldostérone et à l’équilibre glomérulo-tubulaire, d’après H. E. de Wardener.2. Des concepts physiologiques aux réalités pathologiquesLes anomalies tensionnelles notées chez l’homme malade ont des étiologies multiples et des mécanismes physiopathologiques complexes: toute anomalie d’un maillon quelconque d’une régulation entraînant une cascade de réajustements dans l’ensemble des systèmes de contrôle.L’hypotension artérielle peut survenir dans des conditions qu’il est facile de déduire des schémas précédents. Un défaut de remplissage (hémorragie, par exemple), une défaillance de la pompe cardiaque (infarctus du myocarde), une vaso-dilatation périphérique (au cours des maladies fébriles) sont des causes facilement repérées.L’hypotension orthostatique, c’est-à-dire survenant lors du passage de la position allongée à la position debout, évoque une anomalie dans les boucles de la régulation immédiate. On connaît bien à l’heure actuelle l’association d’hypotension orthostatique avec une maladie de Parkinson, l’une et l’autre témoins d’une atteinte des noyaux encéphaliques (syndrome de Shy Drager).L’hypertension artérielle peut s’installer à partir de multiples causes. Il faut savoir distinguer une tumeur de la corticosurrénale (adénome de Conn), une hypersécrétion d’aldostérone, une sténose de l’artère rénale (l’ischémie rénale conduisant à une augmentation de la sécrétion de rénine et à un hyperaldostéronisme fonctionnel consécutif), une sténose de l’isthme aortique; la chirurgie, pratiquée à bon escient, peut apporter la guérison.Le médecin doit savoir reconnaître une intoxication par la réglisse (laquelle contient une substance qui provoque la rétention du sodium), une anomalie génétique enzymatique de la corticosurrénale (que l’on peut bloquer par l’administration de corticoïdes comme la dexaméthazone), voire une pyélonéphrite (infection rénale justiciable des antibiotiques).Mais le plus souvent (dans 60 à 70 p. 100 des cas), il n’y a pas de cause démontrable; l’hypertension artérielle, dite alors essentielle s’inscrit dans une série de dérèglements, assez variables d’un malade à l’autre, mais dans lesquels on peut reconnaître:– Des anomalies du système rénine-angiotensine-aldostérone dont dont nous avons vu le rôle fondamental dans la régulation du stock de sodium de l’organisme. Lorsque rénine et aldostérone sont augmentées, cela correspond le plus souvent à des hypertensions malignes, avec lésions artériolaires importantes et évolution spontanée rapide. Un taux de rénine bas et un taux d’aldostérone normal correspondent à bon nombre d’hypertensions «essentielles»;– Une diminution de la masse plasmatique , assez souvent associée aux anomalies précédentes;– Des anomalies du contrôle neurocirculatoire : l’augmentation du débit cardiaque (surtout fréquente dans l’hypertension labile des sujets jeunes), l’augmentation plus ou moins marquée des résistances périphériques sont notées, en même temps qu’une mauvaise régulation tensionnelle lors du passage du décubitus à la position verticale (épreuve de «tilt»).Compte tenu du tableau assez univoque réalisé par l’ensemble des régulations qui définissent le nouvel équilibre pathologique de l’hypertendu, on conçoit qu’un traitement médical «passe-partout» soit de mise. Il se fonde, d’une part, sur le contrôle des paramètres humoraux, grâce aux diurétiques augmentant l’excrétion du sodium («natriurétiques») et grâce aux inhibiteurs de l’enzyme de conversion qui bloque la formation de l’angiotensine modificateurs du contrôle neurocirculatoire . Il utilise, d’autre part, des médicaments qui interfèrent avec les mécanismes de transmission nerveuse au niveau du système neurovégétatif et des récepteurs qui répondent à son influx (cf. NEUROPHARMACOLOGIE et SYNAPSES).Il reste encore possible de s’opposer à la vaso-constriction en donnant un myorelaxant des fibres lisses (comme l’hydralazine) ou à l’action cardiaque trop énergique (ou à la sécrétion de rénine?) par un 廓-bloqueur, voire de freiner les centres supérieurs par la clonidine.Ces moyens thérapeutiques permettent de normaliser les chiffres tensionnels et de prévenir dans une large mesure, les complications redoutables des maladies hypertensives. Mais leur utilisation nécessite un suivi médical strict et de longue durée.
La tension est donc une force par unité de surface. Quand un médecin parle de tension artérielle, il envisage, en fait, la pression artérielle (P), dont, pour une artère de rayon et d’épaisseur donnés, dépend la tension du vaisseau.Les conceptions cybernétiques permettent une formalisation heuristique. Un système de régulation à court terme utilise les afférences venues de récepteurs à l’étirement (placés dans les sinus carotidiens) pour moduler, à chaque instant, l’activité cardiaque, le degré d’ouverture des vannes artériolaires, la compliance du réservoir veineux.Le remplissage du système circulatoire est contrôlé essentiellement, pour l’eau, par le jeu de l’hormone antidiurétique (réglé à partir d’osmorécepteurs et de volorécepteurs) et, pour le sodium, par l’intervention de l’aldostérone, hormone corticosurrénale dont la sécrétion est, en grande partie, asservie au taux d’angiotensine fabriquée par une enzyme d’origine rénale: la rénine.Les connaissances physiologiques acquises permettent désormais de remédier directement aux causes de l’hypertension artérielle et, dans la grande majorité des cas, d’opposer des médications efficaces à cette anomalie physiopathologique aux conséquences redoutables.1. Physiologie de la pression artérielleHistoriqueIl a fallu plus de cent ans, après que Harvey eut découvert la circulation du sang (1628), pour que S. Hales mesure pour la première fois la pression artérielle (1730), grâce à un tube de verre relié à une canule placée dans l’artère crurale d’une jument; un autre siècle s’écoule avant que J. L. M. Poiseuille applique à l’étude de la pression artérielle sanguine le manomètre à mercure (1828); la notion de pression était déjà bien précisée (une force rapportée à une surface) et, aujourd’hui encore, les physiologistes ont conservé l’habitude d’évaluer en millimètres de mercure plutôt qu’en unités C.G.S.C. F. Ludwig, vers 1847, met au point le «kymographion», qui permet de tracer le graphe de la pression artérielle (en millimètres de mercure) en fonction du temps. E. J. Marey et A. Chauveau, vers 1860, inventent les dispositifs qui rendent possible l’étude des variations de pressions à l’intérieur de l’appareil circulatoire. L’époque contemporaine a vu enfin la réalisation de capteurs convertissant l’énergie mécanique en signaux électriques auxquels on peut faire subir toutes les transformations qu’implique maintenant le traitement de l’information (P. Laurens).Chez l’homme, les méthodes de mesure non sanglante de la pression artérielle (par l’intermédiaire de la contre-pression instituée sur les troncs artériels des membres grâce à un brassard de caoutchouc gonflable) font partie de la routine clinique. Les méthodes palpatoires de S. Riva Rocci (1896), oscillatoires de V. Pachon (1909) sont moins utilisées que la méthode auscultatoire de P. Korotkow (1905) qui s’appuie sur l’étude des caractéristiques des bruits artériels synchrones avec la pulsation artérielle. Ces diverses méthodes mesurent en fait l’aptitude de la paroi vasculaire à équilibrer (par son élasticité) la pression sanguine: elles permettent ainsi d’évaluer la pression artérielle et de mettre en évidence ses variations normales et pathologiques.Données physiologiquesLes variations de la pression artérielleOn résumera ici les faits exposés déjà dans l’article appareil CIRCULATOIRE. Si l’on enregistre simultanément une courbe de pression intraventriculaire gauche et l’électrocardiogramme, on constate la succession des phénomènes suivants:– l’onde rapide Q.R.S.T. de l’électrocardiogramme (50 ms) précède tous les phénomènes mécaniques;– pendant la contraction isométrique ventriculaire (50 ms), la pression intraventriculaire croît sans que la pression aortique monte;– pendant la période d’éjection ventriculaire (220 ms), les courbes ventriculaires et aortiques coïncident: la pression aortique maximale peut être identifiée à la pression systolique ventriculaire;– la pression aortique décrit un ressaut (l’incisure) à la fin de l’éjection ventriculaire: la fermeture des sigmoïdes aortiques sépare les régimes de pression aortique et ventriculaire; là commence la diastole cardiaque; la pression aortique décroît progressivement jusqu’à un minimum qui coïncide avec la fin de la diastole cardiaque et pour cette raison est appelée pression diastolique.À ces oscillations de premier ordre se superposent des oscillations de deuxième ordre en rapport avec les mouvements respiratoires, et les oscillations dites de Traube-Hering qui surélèvent l’ensemble du tracé à une fréquence beaucoup plus lente (W. D. Halliburton).Modifications de la pression sanguine dans l’appareil circulatoireChez l’homme, les performances sont obtenues grâce à la convexion forcée que réalise la pompe cardiaque à l’intérieur de la tuyauterie vasculaire en circuit fermé.En suivant le circuit circulatoire, on peut distinguer un certain nombre de segments à propriétés très contrastées (cf. appareil CIRCULATOIRE, fig. 9).Le compartiment à haute pression commence avec le ventricule gauche (lors de la systole) et s’étend jusqu’aux artérioles. Ce compartiment contient seulement une faible proportion du volume sanguin (environ 15 p. 100); son volume ne dépend pas du volume sanguin total mais de celui qui est éjecté à la systole par le ventricule gauche et de l’élasticité des vaisseaux ; il présente une faible compliance (la compliance est définie, grâce au nombre de litres mobilisés par une variation de pression unité); il est drainé par des systèmes artériolaires, disposés en parallèle, dont la résistance est réglée par l’action de cellules musculaires lisses.Il semble que la stabilisation de la pression artérielle ait pour but téléonomique la perfusion correcte des organes nobles «servis et non asservis», le cœur et le cerveau, aux dépens de la fermeture éventuelle d’autres shunts artério-veineux.Viennent ensuite le compartiment de distribution capillaire et cellulaire et le compartiment à basse pression qui contient environ 80 p. 100 du volume sanguin: 55 p. 100 dans les veines et les veinules; le reste, soit 25 p. 100 de la masse sanguine, dans le cœur droit, les poumons et l’oreillette gauche.Interprétation cybernétiqueDepuis que les travaux de Wiener sur la cybernétique ont formalisé l’idée de rétro-action, les physiologistes se sont efforcés de formaliser la structure logique du système de régulation de la pression artérielle.Supposons, dans un premier temps, que le remplissage du système schématisé dans la figure 1 soit convenable et stable: la pression artérielle est la grandeur réglée à l’intérieur du système (en trait gras); elle dépend de l’interaction entre la pompe cardiaque, qui réalise la charge du système, et le calibre des artérioles, qui décide du débit de drainage. Soit un capteur sensible à l’étirement situé dans l’intimité de la paroi du système réglé qui renseigne à chaque instant un système comparateur (comportant une grandeur de consigne GC): ce sera la boucle de rétroaction négative du système cybernétique. L’écart entre la grandeur de consigne et la grandeur mesurée par le capteur constitue l’information qui permet au contrôleur d’asservir pompe cardiaque et résistances artériolaires.Aux «entrées utiles», réseau de communication qui unit le système de contrôle aux deux effecteurs cardiaque et vasculaire constituant le système réglant, s’opposent des «entrées parasites» qui peuvent, à chaque instant, déséquilibrer l’ensemble. Les entrées sont liées à l’activité cellulaire, glandulaire ou musculaire, aboutissant à la synthèse d’un certain nombre de substances vaso-activesdites «autacoïdes» par Sharpey Schafer (sérotonine, histamine, prostaglandines). C’est probablement par l’intermédiaire de telles substances (et aussi de la pression artérielle de gaz carbonique) que les circulations locales «négocient» les données imposées par la régulation générale, qui doit alors, par le jeu des rétroactions, déterminer un nouvel équilibre.Régulation «immédiate» de la pression artérielleAnalyse des afférences barosensibles: les nerfs dépresseursEn 1867, E. de Cyon et C. F. Ludwig découvrent un «nerf dépresseur» (fig. 2); prenant son origine au niveau de la crosse aortique et dont l’excitation détermine bradycardie et hypotension. Mais ce sont les travaux de H. E. Hering (1924) qui apportent les repères essentiels. La compression du sinus carotidien détermine une chute de la pression sanguine avec ralentissement du rythme cardiaque; ces phénomènes ne se produisent pour aucun autre segment des carotides. Les mêmes résultats sont obtenus par étirement des sinus de dedans en dehors par un ballonnet ou par augmentation de la pression sanguine à l’intérieur du sinus. Les terminaisons des nerfs de Hering ne sont pas sensibles directement à la pression; si l’on entoure la paroi du sinus d’une feuille de plomb, les modifications de pression à l’intérieur ne déterminent plus de réponse; les récepteurs sont des récepteurs à la distorsion de la paroi. Tous ces effets sont abolis par la section d’un rameau nerveux (appelé ordinairement nerf de Hering) qui joint le sinus carotidien au glosso-pharyngien. La stimulation du bout central de ce nerf entraîne les mêmes effets que la déformation de la paroi du sinus.Si l’on coupe les nerfs de Cyon et les nerfs de Hering, la pression artérielle s’installe (comme Hering l’a montré pour le chien) à un niveau très élevé. Il faut admettre qu’à chaque instant ces nerfs exercent une action dépressive sur le système cardio-vasculaire, ils sont bien les «rênes de la pression sanguine» (Blutdruckzügler ).Étude des «ripostes»Si l’on déclenche la réaction du système «à boucle ouverte» en excitant le nerf du sinus ou en distendant le sinus, selon la technique de J. Heymans, cette réaction s’exerce au niveau des deux systèmes asservis: la pompe cardiaque, les shunts artériolaires (fig. 2).La pompe cardiaque est douée d’une parfaite autonomie: un cœur isolé dans des conditions convenables conserve son activité rythmique et mécanique et s’adapte au débit qui lui est apporté (cf. infra ). Mais, dans l’organisme entier, il est asservi par l’intermédiaire des neuromédiateurs que lui délivrent les systèmes parasympathiques (nerfs pneumogastriques ou vagues) et orthosympathiques (avec le relais médullo-surrénal). La vagotomie, ou l’administration d’atropine, empêche le ralentissement cardiaque déclenché par l’excitation du nerf du sinus carotidien; celle-ci inhibe, d’autre part, l’accélération du rythme cardiaque par les nerfs cardiaques orthosympathiques. Au contraire, la section des nerfs du sinus les empêche de réfréner l’activité orthosympathique qui, par l’intermédiaire des récepteurs cardiaques de type 廓 (c’est-à-dire bloqués électivement par des drogues du type propanolol), aboutissent à l’accélération du cœur et à l’augmentation de la force de ses battements.Les artérioles , de leur côté, sont douées d’autorégulation probablement myogène (B. Folkow): toute augmentation brusque de la perfusion d’une artère isolée in vitro détermine une réponse constrictrive, peut-être par le truchement de certaines cellules musculaires de la paroi du vaisseau; douées d’autonomie, elles ont été appelées «unitaires» (E. Bozler). Mais, en dehors de ces phénomènes d’autorégulation, la plupart des cellules musculaires du vaisseau (dites multi-unitaires) sont asservies par le truchement de fibres végétatives. Le rôle essentiel en matière de réponse vaso-motrice, à la suite de la distension des sinus, est joué par la diminution du tonus vaso-constricteur que maintient la noradrénaline libérée par les terminaisons orthosympathiques au contact des alpha-récepteurs des fibres musculaires lisses des artérioles (rappelons que ces récepteurs sont bloqués par l’ergotoxine et la phentolamine). Les fibres vasodilatatrices (orthosympathiques cholinergiques) ne participent pas à cette régulation (B. Folkow et B. Uvnäs).Reste à situer l’importance du réservoir veineux : une diminution du calibre veineux, par exemple, va augmenter le retour veineux au niveau du cœur et déterminer l’allongement des fibres cardiaques et la réponse adaptée, propre à ces fibres. Ce mécanisme d’ajustement, fonction de la longueur diastolique des fibres, est un ajustement a posteriori, curatif, qui peut s’ajouter au contrôle homéométrique préventif réalisé (cf. supra , Interprétation cybernétique ) par le truchement des catécholamines sécrétées par le système végétatif.De toute façon, le contrôle neurovégétatif découle de l’activité de centres nerveux spécialisés. On peut mettre en évidence leur localisation et leur rôle par ablation localisée ou par stimulation (avec le risque d’obtenir des réponses par des voies qui ne sont pas physiologiques). On met ainsi en évidence des centres bulbaires (noyaux des IXe et Xe paires crâniennes en particulier), suprabulbaires et médullaires. Au niveau de ces nerfs reliés à ces centres, les ganglions latérovertébraux sont le siège des relais synaptiques. La médullo-surrénale représente, pour le nerf grand-splanchnique, l’équivalent de cellules ganglionnaires qui sécrètent les catécholamines (adrénaline surtout) dans le système circulatoire par lequel elles gagnent la pompe cardiaque et les drains artériolaires.On peut imaginer a priori que l’ajustement réflexe varie soit en fonction d’un «resetting» de la valeur de consigne décidé au niveau des centres par le contrôleur (fig. 1), soit en fonction de modifications des propriétés mécaniques de la paroi des sinus.Régulation du remplissageEn fonction de la diurèse nécessaire à l’activité rénale, des pertes par perspiration cutanée et respiratoire, la «masse sanguine» varie. Une modulation de la fonction rénale et du ravitaillement oral va la régler suivant des mécanismes «à long terme» (à grande constante de temps). Le «remplissage» (fig. 3) concerne essentiellement le compartiment compliant, c’est-à-dire l’ensemble de la tuyauterie vasculaire, à l’exception du cœur gauche en systole et du système artériel dont on a étudié la régulation. L’osmolarité et la volémie sont réglées en même temps, mais, s’il le faut, l’osmolarité est sacrifiée au maintien de la volémie.Hormone antidiurétique et eauDepuis E. B. Verney, on sait que l’on bloque la diurèse déterminée par un apport d’eau par voie buccale en injectant une faible quantité de solution salée hypertonique dans la carotide (sans action par une autre voie). On a reconstruit (fig. 3) le circuit qui, par le jeu d’osmorécepteurs (a ), met en route la sécrétion, par des neurones supraoptiques, d’hormone antidiurétique (ADH), libérée au niveau de la posthypophyse dans le torrent circulatoire pour agir au niveau du tube distal du néphron [cf. REIN] en favorisant la réabsorption d’eau. Ainsi est rétablie par feed-back négatif l’osmolarité normale. Ce contrôle de l’osmolarité par le jeu de l’ADH est coiffé par des volorécepteurs, certains situés dans la veine cave (réflexe de Bainbridge, b ), d’autres (discutés) dans l’oreillette et dans le ventricule (réflexe de Bezold Jarisch, b -b ). Mais les plus importants sont ceux situés dans l’oreillette gauche (c ) et décrits par O. J. Gauer et J. P. Henry. Ces capteurs de l’oreillette gauche sont excités par la distension suivant un mécanisme analogue à celui que nous avons vu au niveau du sinus carotidien. Les informations cheminent cette fois-ci par la voie afférente du pneumogastrique: au niveau des centres supraoptiques l’embargo est mis sur l’exportation d’ADH. Se déclenche ainsi une diurèse qui empêche que la pression ne favorise, dans le secteur intrathoracique, une exsudation œdémateuse au niveau des alvéoles pulmonaires.Systèmes aldostérone et sodium. Systèmes rénauxOn sait, depuis Tigerstedt et Bergman, (1898) que le rein règle la pression artérielle par l’intermédiaire d’une substance humorale, la rénine. Les travaux des écoles de I. H. Page (1939) et de E. Braun-Ménendez (1940) ont montré que la rénine est une enzyme qui agit sur une 見-2-globuline plasmatique pour fabriquer un décapeptide, l’angiotensine I , que la traversée pulmonaire transforme en un octapeptide de structure chimique connue: l’angiotensine II. Il y a tout lieu de penser que ce sont certaines cellules myocytaires à granules cytoplasmiques de l’artère afférente du glomérule qui sécrètent la rénine. Tout se passe comme si de la diminution de la pression artérielle provoquant l’excitation sécrétoire des cellules à granules résultait une concentration plus élevée de rénine, c’est-à-dire d’angiotensine. Celle-ci est non seulement une substance artériolo-constrictrice, mais, de plus, elle déclenche, comme J. Genest, puis J. H. Laragh l’ont démontré, la sécrétion d’aldostérone par le cortex surrénalien. Sous l’action de l’aldostérone sécrétée, le tube contourné distal réabsorbe davantage de sodium conduisant à l’inflation du compartiment extracellulaire, vasculaire en particulier, c’est-à-dire au rétablissement d’une «pression normale».D’autres facteurs agissent au niveau du rein et contribuent à cette régulation: l’équilibre ou «balance» glomérulo-tubulaire; l’intervention constrictrice de prostaglandines sur l’artère efférente du glomérule et l’action natriurétique d’un éventuel «troisième facteur», s’ajoutant à l’aldostérone et à l’équilibre glomérulo-tubulaire, d’après H. E. de Wardener.2. Des concepts physiologiques aux réalités pathologiquesLes anomalies tensionnelles notées chez l’homme malade ont des étiologies multiples et des mécanismes physiopathologiques complexes: toute anomalie d’un maillon quelconque d’une régulation entraînant une cascade de réajustements dans l’ensemble des systèmes de contrôle.L’hypotension artérielle peut survenir dans des conditions qu’il est facile de déduire des schémas précédents. Un défaut de remplissage (hémorragie, par exemple), une défaillance de la pompe cardiaque (infarctus du myocarde), une vaso-dilatation périphérique (au cours des maladies fébriles) sont des causes facilement repérées.L’hypotension orthostatique, c’est-à-dire survenant lors du passage de la position allongée à la position debout, évoque une anomalie dans les boucles de la régulation immédiate. On connaît bien à l’heure actuelle l’association d’hypotension orthostatique avec une maladie de Parkinson, l’une et l’autre témoins d’une atteinte des noyaux encéphaliques (syndrome de Shy Drager).L’hypertension artérielle peut s’installer à partir de multiples causes. Il faut savoir distinguer une tumeur de la corticosurrénale (adénome de Conn), une hypersécrétion d’aldostérone, une sténose de l’artère rénale (l’ischémie rénale conduisant à une augmentation de la sécrétion de rénine et à un hyperaldostéronisme fonctionnel consécutif), une sténose de l’isthme aortique; la chirurgie, pratiquée à bon escient, peut apporter la guérison.Le médecin doit savoir reconnaître une intoxication par la réglisse (laquelle contient une substance qui provoque la rétention du sodium), une anomalie génétique enzymatique de la corticosurrénale (que l’on peut bloquer par l’administration de corticoïdes comme la dexaméthazone), voire une pyélonéphrite (infection rénale justiciable des antibiotiques).Mais le plus souvent (dans 60 à 70 p. 100 des cas), il n’y a pas de cause démontrable; l’hypertension artérielle, dite alors essentielle s’inscrit dans une série de dérèglements, assez variables d’un malade à l’autre, mais dans lesquels on peut reconnaître:– Des anomalies du système rénine-angiotensine-aldostérone dont dont nous avons vu le rôle fondamental dans la régulation du stock de sodium de l’organisme. Lorsque rénine et aldostérone sont augmentées, cela correspond le plus souvent à des hypertensions malignes, avec lésions artériolaires importantes et évolution spontanée rapide. Un taux de rénine bas et un taux d’aldostérone normal correspondent à bon nombre d’hypertensions «essentielles»;– Une diminution de la masse plasmatique , assez souvent associée aux anomalies précédentes;– Des anomalies du contrôle neurocirculatoire : l’augmentation du débit cardiaque (surtout fréquente dans l’hypertension labile des sujets jeunes), l’augmentation plus ou moins marquée des résistances périphériques sont notées, en même temps qu’une mauvaise régulation tensionnelle lors du passage du décubitus à la position verticale (épreuve de «tilt»).Compte tenu du tableau assez univoque réalisé par l’ensemble des régulations qui définissent le nouvel équilibre pathologique de l’hypertendu, on conçoit qu’un traitement médical «passe-partout» soit de mise. Il se fonde, d’une part, sur le contrôle des paramètres humoraux, grâce aux diurétiques augmentant l’excrétion du sodium («natriurétiques») et grâce aux inhibiteurs de l’enzyme de conversion qui bloque la formation de l’angiotensine modificateurs du contrôle neurocirculatoire . Il utilise, d’autre part, des médicaments qui interfèrent avec les mécanismes de transmission nerveuse au niveau du système neurovégétatif et des récepteurs qui répondent à son influx (cf. NEUROPHARMACOLOGIE et SYNAPSES).Il reste encore possible de s’opposer à la vaso-constriction en donnant un myorelaxant des fibres lisses (comme l’hydralazine) ou à l’action cardiaque trop énergique (ou à la sécrétion de rénine?) par un 廓-bloqueur, voire de freiner les centres supérieurs par la clonidine.Ces moyens thérapeutiques permettent de normaliser les chiffres tensionnels et de prévenir dans une large mesure, les complications redoutables des maladies hypertensives. Mais leur utilisation nécessite un suivi médical strict et de longue durée.
Encyclopédie Universelle. 2012.
